SOLUCIONES AL TEMA 2
2.1
a)
d= m / V =
(132,91+35,45) g / mol / 6,023*1023 mol-1 * l3
= 3,99 g / cm3
Obsérvese que hay 1 Cs+
y 8*1/8 (=1) Cl- por celdilla. Si despejamos obtenemos :
l3 = 7,006*10-23 cm3 ;
l = 4,12*10-8 cm = 4,12 .
b)
d2 = l2 + l2 + l2 =
3*(412 pm) 2
d = 713 pm
rCs++rCl- = 713 / 2 = 357 pm
c)
d Cs+-Cs+ = d Cl
- Cl = l = 412 pm
d)
rCs++ rCl-
= 357 pm rCs+ = 357 - 180 = 177 pm
![]()
2.2
d = 2,16 g / cm3
l = 3,00 cm
![]()
2.3 0,033 defectos Schottky por
celdilla.
![]()
2.4
a) Pd H0,2
b) 252,6 L
c) 2,75
![]()
2.5
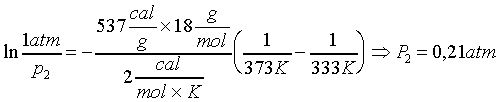 .
.
![]()
2.6
a.-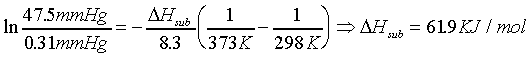
b.- 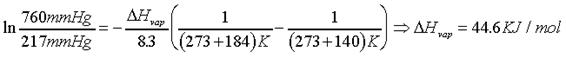
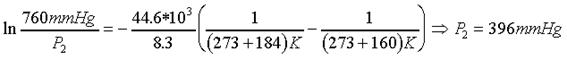
c.- 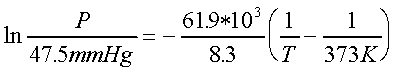
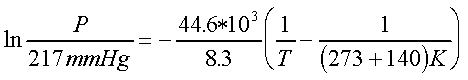
Si despejamos obtenemos
los valores de la presión y la temperatura del punto triple que son :
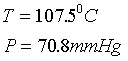
d.- 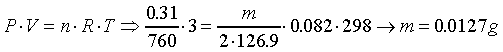
Como sólo hay 10 mg, se
evaporan esos 10 mg
![]()
2.7
Hay en el aire de la habitación 419 g de agua
Se evaporan del barreño 279 g de agua.
![]()
2.8
a) 8 átomos / celdilla
b) 5,43 Å
c) 34 % en los dos
casos
![]()